Le compost, un outil de biotechnologie
Qu'est ce que le compost ?
Le compost est un mélange de déchets organiques principalement dont on se sert pour l'agriculture. Le compost sert de nutriments aux plantes. On a pu constater que dans le compost, il y a des bactéries. Ces bactéries peuvent transformer les déchets organiques en nutriments de qualités pour les plantes grâce à des réactions chimiques. Nous avons fait une expérience pour comprendre d'où ces bactéries pouvaient provenir.
D'où viennent les bactéries ?
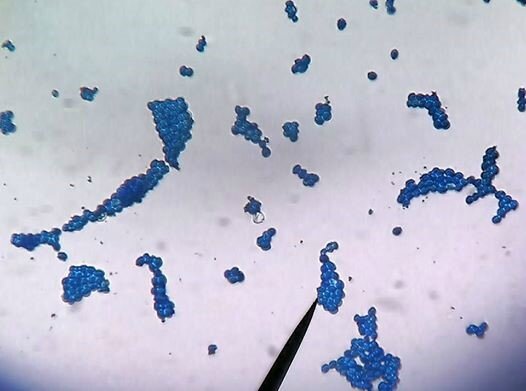
Nous avons mis en culture sur des géloses nutritives ordinaires de l'eau de pluie, des déchets organiques de poubelle (peau de banane), de la terre ou de l'air. Nous avons laissé nos géloses pendant une semaine a température ambiante pour observer les bactéries présentes après culture. Nous avons obtenu les résultats suivants.
Nous en avons conclu que les bactéries se retrouvaient essentiellement dans la terre, sur les déchets et dans l'eau.
Quelle est l'efficacité du compost ?
Pour cette expérience il nous a fallu le matériel nécessaire à la culture de graines : un pot, un support, de la terre, du compost et des graines (radis ou basilic).
Nous avons testé trois conditions :
- la terre seule
- le compost seul
- un mélange 50/50 de terre et de compost mélangé de façon homogène.
Ensuite, nous avons déposé les graines puis nous avons arrosé nos plantations. Nous les avons laissées pousser une semaine.
Observations des plants de radis au bout de 7 jours
Au bout d'une semaine seule les plans de radis avaient poussé. Nous avons donc laissé une semaine de plus nos cultures. Dans tous les cas nous avons réussi à faire germer nos graines mais nous n'avons pas observé de différences significatives. Nous aurions pu faire une optimisation du protocol pour pouvoir être plus rigoureux sur l'analyse à faire : peut être fallait il réfléchir au choix des plantes. Nos plantes étaient facile à cultiver donc peut être que le radis n'avait simplement pas besoin d'améliorer sa germination. Peut être qu'en laissant les légumes pousser on se serait rendu compte que le compost permettait d'avoir des légumes de meilleur qualité.
Le compost ne semble pas avoir d'impact sur la quantité de graîne germée mais peut être qu'il en aurait sur la qualité de la production.